Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (26): 4259-4264.doi: 10.3969/j.issn.2095-4344.0762
Acellular tissue matrix in plastic surgery: research progress and clinical application
Yang Mei-rong1, Pan Bo1, Zhao Bo2
- 1Plastic Surgery Hospital, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100144, China; 2Beijing Biosis Healing Biological Technology Co., Ltd., Beijing 102600, China
-
Received:2018-01-19 -
Contact:Pan Bo, Chief physician, Professor, Doctoral supervisor, Plastic Surgery Hospital, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100144, China -
About author:Yang Mei-rong, Doctoral candidate, Plastic Surgery Hospital, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100144, China -
Supported by:the National High-Technology Research and Development Program of China (863 Program), No. 2015AA033602; Small- and Mid-sized Enterprise Technology Innovation Fund, No. Z14010101281
CLC Number:
Cite this article
Yang Mei-rong, Pan Bo, Zhao Bo. Acellular tissue matrix in plastic surgery: research progress and clinical application[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(26): 4259-4264.
share this article

2.1 脱细胞基质材料的分类 脱细胞基质材料是在细胞外基质成分与结构的基础上,通过脱细胞工艺去除细胞而保留其生物活性成分的基质材料,是含有多种信号分子构成高度协调的有机统一体,能够诱导并促进细胞的黏附、增殖、分化及组织形成,是机体组织修复的基础[4]。刘文博等[5]根据不同来源组织生物活性成分的差异,将脱细胞基质材料分为两类:①惰性组织源材料:以人尸/猪的真皮、牛/猪/马的心包、牛/猪的腹膜等为代表。来源组织虽然保留组织三维超微结构,但是组成成分无生物活性成分,仅能诱导血管化的结缔组织再生填充组织缺损、实现解剖层面的修复。由于惰性组织源材料含有大量降解缓慢,人体无法降解吸收弹性纤维,可导致修复区远期变形,易形成收缩性瘢痕化修复区域[6-7];②细胞外基质源材料:不仅保留了完整的三维超微结构,并且保留了多种生物活性成分。这类产品以猪小肠黏膜下层、猪膀胱黏膜层基底膜、人羊膜等为代表。细胞外基质源材料植入后可以主动诱导和促进周围细胞的迁入、黏附、增殖和分化,迁入的细胞进一步对材料进行改造、降解和塑形,实现组织的形成和结构重塑[8](表1)。"

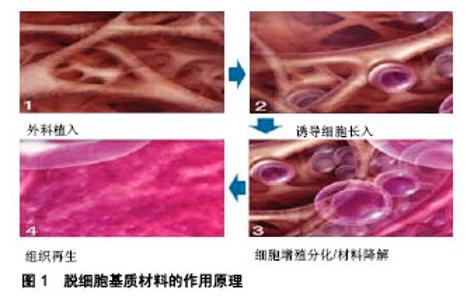
2.2 脱细胞基质材料作用原理 脱细胞基质材料修复缺损促进组织再生基质机制是“内源性诱导再生”,胶原纤维形成三维多孔连通网络结构,为细胞迁移、长入、 合成新生胶原蛋白提供物理微环境,而保留细胞外基质中的各种活性成分与生长因子,促进组织修复,重塑血管化、功能化的组织与器官,实现迁入的细胞进一步对材料进行改造、降解和塑形,实现组织的形成和结构重塑[4,8](图1)。而非降解吸收材料植入体内后主要通过异物刺激、慢性炎症反应机制,形成纤维化包裹,形成结构瘢痕组织来替代缺损组织,其修复原理与细胞外基质源脱细胞基质材料是两种不同生物学过程[9]。 脱细胞基质材料植入后再血管化速度快,吞噬细胞能早期进入材料内部,细菌生物被膜难以形成,较非降解吸收材料更耐受感染[10]。由于在诱导组织再生与耐受感染两个方面具有突出优势,脱细胞基质材料受到整形外科领域专家重视,特别是细胞外基质源材料还能实现组织部分程度的特异性、功能性修复,具有巨大的临床使用价值。 2.3 脱细胞基质材料的免疫原性 脱细胞工艺是去免疫原性技术的核心,也是脱细胞基质材料制备工艺的关键和难点。近十年来组织脱细胞方法一直在不断的发展和改良,研究的重点是清除细胞成分的同时,保护天然细胞外基质的生物性能和力学性能,并且无有害物质残留。脱细胞方法分为物理方法、化学方法和酶法。物理方法包括机械震荡、反复冻融、高压、超声波振荡等,上述物理方法的作用机制多为直接破坏细胞膜,使细胞内容物释出。常用的化学试剂包括酸碱、离子型或非离子型去垢剂、交联剂、螯合剂等无机或有机试剂,其作用机制包括破坏细胞间或细胞与细胞外基质间连接,溶解细胞质成分,破坏细胞内核酸、蛋白、脂质间的连接等,常用的酶包括各种核酸酶和蛋白酶,其作用机制是通过对核酸和蛋白的水解作用,清除DNA,破坏细胞间或细胞与细胞外基质间的连接。 机械震荡、超声波振荡等物理方法对细胞外基质的影响较小,但细胞成分残留较多,且无法清除DNA成分,大部分组织需要结合化学方法或酶法清除细胞内容物和细胞碎片。而去垢剂、酸碱、交联剂、螯合剂等化学试剂和各种酶类均会不同程度地破坏细胞外基质的结构和成分,特别是胶原蛋白、葡胺聚糖及各种生长因子,并且,有机溶剂、交联剂和酶类往往难以有效清除,造成材料中的残留,引起细胞毒性或免疫反应。 对已上市的异种脱细胞基质材料的临床结果分析表明,现有的产品均不同程度存在浆液肿、感染、免疫排斥反应、组织愈合不良等并发症[11-12]。异种动物来源脱细胞基质材料的免疫原性主要来源于α-半乳糖苷酶,当脱细胞基质材料残留有α-半乳糖苷酶并植入人体后,会激发产生抗α-半乳糖苷酶免疫球蛋白,包括IgG、IgM,从而出现特异性免疫反应及体内纤维包裹、组织钙化[13]。 然而,脱细胞基质材料中免疫原性可通过制备工艺优化,降低、去除基质中α-半乳糖苷酶含量,降低免疫原反应风险。不同的脱细胞工艺对α-半乳糖苷酶清除率效果影响较大,Wu等[14]通过优化脱细胞工艺去除α-半乳糖苷酶,结果表明其清除率约为77.8%,Wong等[15]报道α-半乳糖苷酶清除率为89.1%。 因此,作为整形外科填充材料,脱细胞基质材料中免疫安全性指标需要进一步严格控制,以保证材料的安全性。 2.4 脱细胞基质材料在整形外科的应用 2.4.1 烧伤创面愈合修复 伤口愈合是人类生命中发生的最复杂和最有活力的生物过程之一[16-17]。临床上大面积烧伤属于常见现象,而对于处理烧伤部位皮肤愈合是一大难题。因为比较严重的烧伤涉及的皮肤真皮层已基本消失殆尽,虽然通过刃厚小皮片或者微粒植皮技术能够使创面愈合,但愈合后的创面存在弹性差、凹凸不平等问题,导致愈合效果极差。而采用自体移植皮瓣或者全厚及中厚皮片虽然能够解决以上问题,但容易造成供区缺损,这实际上是一种瘢痕的移位,而没有从根本上解决问题。而脱细胞真皮基质的广泛应用,对促进烧伤的皮肤愈合意义重大。 脱细胞基质材料最早应用于大面积烧伤切痂创面的修复上,发现能有效减少瘢痕形成和皮片收缩。Wainwright等[18]应用脱去细胞成分的异体真皮与网状自体薄皮片复合移植修复深度烧伤创面,术后经组织学观察上皮细胞覆盖良好,瘢痕增生较少。国内临床研究也表明,将异种脱细胞基质材料与自体皮肤进行复合移植治疗深度烧伤创面,不仅显著减轻了愈合后瘢痕的形成,并且提高了愈合后的皮片质量,同时具有供皮区损伤小、恢复快、无瘢痕等特点,是修复深度烧伤创面的一种较好皮肤修复材料[19-21]。除此之外,黄智勇等[22]还将脱细胞基质材料用于烧伤后期瘢痕挛缩畸形的修复,取得了良好效果。 2.4.2 慢性创面及病理性瘢痕的修复 除作为支架材料应用于烧伤创面外,许多学者还将脱细胞基质材料应用到慢性创面及病理性瘢痕的整形修复上。霍然等[23]应用脱细胞真皮基质一期覆盖胸部瘢痕疙瘩切除后的创面12例,二期应用自体刃厚皮片移植于脱细胞真皮基质上,效果满意。12例脱细胞真皮基质和刃厚皮片均大部分成活,无失败病例。术后11例3个月至2年随访中,胸部瘢痕疙瘩无复发,术区皮肤质地相当于中厚皮片。Gibbs等[24]将脱细胞基质材料应用到慢性创面、增生性瘢痕等的整形修复上亦收到了与自体中厚或全厚皮片移植同样的修复效果。Godwin等[25]也通过对高度再生的生物体如斑马鱼和蝾螈的研究发现,细胞外基质成分在能够支持修复和再生的同时避免了瘢痕形成。 2.4.3 乳房重建 乳腺癌发病率日益上升,据世界卫生组织统计数据显示,仅2012年全球新增乳腺癌病例数大约167.7万[26]。随着乳房切除术数量的增加和审美意识的提高,对乳房重建手术的需求也增加。在一期假体植入乳房重建术中,胸大肌难以完全覆盖假体且术中不能实现乳房下皱襞的重建,乳房形态欠佳。Dong等[27]利用脱细胞真皮基质加宽和延长胸大肌,使得胸大肌后间隙增大,从而将假体完全覆盖,同时重建乳房下皱襞,乳房形态良好。 Jin等[28]在植入式乳房重建兔模型中发现,用脂肪细胞来源干细胞接种的脱细胞真皮基质显示出诱导血管生成并改善伤口愈合。Nafisi等[29]在羊模型中应用脱细胞真皮基质进行乳房重建评估,组织学评估结果显示:所有植入的脱细胞真皮基质均有成纤维细胞的生长和血运重建,并且皮肤和乳腺附近的脱细胞真皮基质植入也有效降低了手术并发症的整体发生率。而这一结果进一步提示脱细胞真皮基质有望发展在植入前不需要进行皮肤扩张的乳房重建。Spear等[30]通过回顾5年内118例使用脱细胞真皮基质行乳房重建患者的资料,发现脱细胞真皮基质是一种可靠的修复材料,可以增加植入体的乳房重建成功性并降低整体并发症的风险。Long等[31]在评估脱细胞真皮基质结合植入物矫正聚丙烯酰胺水凝胶移除后的继发畸形分析中发现,脱细胞真皮基质和植入物都可以安全地矫正继发畸形。Paprottka等[32]对乳房重建使用源自人类、猪或牛来源的脱细胞真皮基质产品进行长期随访研究发现,脱细胞真皮基质植入后的并发症发生率为17%(源自人类:7%,源自猪:14%,源自牛:31%)。Zenn等[33]在研究中指出尽管目前的证据表明使用脱细胞真皮基质可能会增加某些并发症(感染、血清肿瘤)的风险,但选择合适的患者可最大限度地减少或消除这些风险。Krishnan等[34]通过对乳房重建中具有和不具有脱细胞真皮基质的两阶段研究,探索脱细胞真皮基质在乳房重建过程中的成本效用分析。实验结果提示:在脱细胞真皮基质的人群中,植入物的质量生命年增加为1.37,而成本效益的增量与成本效用比为264.20美元/质量生命年。单因素敏感性分析证实,即使单侧和双侧乳房重建使用的是脱细胞真皮基质材料的零售成本,使用脱细胞真皮基质也具有成本效益。因此即使脱细胞基质材料的使用使成本增加,但由于其在乳房重建术中的效用增加,所以脱细胞真皮基质是一种成本效益高的技术。 2.4.4 软骨组织修复填充 在重建填充软骨组织时,制造出非常类似于天然软骨组织的微环境支架仍然是一个主要的挑战[35]。Luan等[36]关于脱细胞软骨基质对软骨细胞体外生长影响的研究表明,异体脱细胞软骨基质可提供适宜于软骨细胞生长的良好环境,提示脱细胞细胞外基质材料在软骨组织工程中的广阔前景。Zhang等[37]对脱细胞软骨基质作为支架材料进行了研究,实验研究将18只新西兰白兔分为3组,在每只兔耳朵中切下两片 1 cm×1 cm的软骨,缺损修复情况如下:A组为脱细胞软骨基质和软骨膜联合移植,B组为脱细胞软骨基质,C组为软骨膜。其实验所得结论是脱细胞软骨基质是软骨组织工程的潜在支架材料。 2.4.5 面部整形及美容 唇腭裂修复:Clark等[38]将异体脱细胞真皮基质用于7例唇腭裂患者的腭成形中,术后随访7例均表现为脱细胞真皮基质上皮化且与伤口融合,无穿孔,无局部炎症与感染,形成瘢痕及瘢痕挛缩程度与周围瘢痕相比未见明显差异。Cole等[39]将脱细胞基质材料用于唇腭裂修复术后口鼻瘘的修复,术后随访口鼻瘘及鼻反流等症状均无复发。 鼻部整形修复:与西方人相比,亚洲人群的鼻部都显得低矮平塌,而鼻头圆钝、肥厚,所以亚洲人要求鼻部整形的越来越多。创伤、骨折等后天原因亦可导致鼻部畸形,因而临床整形医生在选择填充材料时需要进行多方面考虑,以求能获得患者术后的满意度。李光强等[40]将脱细胞异体真皮基质医用补片应用于隆鼻术中并获得了较高的满意度。一方面,其组织相容性优于硅胶、膨体,能够使患者获得手感自然、更加挺拔、完全自体化的鼻尖。另一方面,植入物会随着植入的时间而使轮廓凸显,而这也是进行鼻修复手术的重要原因。在鼻修复中,通常脱细胞真皮基质会位于皮肤包膜和植入物之间。Suh等[41]研究将覆有脱细胞真皮基质的硅胶材料植入大鼠体内后,组织学发现脱细胞真皮基质的存在,使得植入物周围的包膜厚度和肌成纤维细胞活性显著降低。Jackson等[42]和Gryskiewicz等[43]将脱细胞基质材料用于鼻部畸形的矫正,术后鼻外形得到改善。 眼部畸形修复:临床上常见的眼睑部缺损修复方法有自体皮片、皮瓣或复合组织移植修复,但术后效果欠佳,且会造成新的畸形。Shorr等[44]运用脱细胞基质材料修复63例眼部畸形患者,修复后移植物无排斥及毒性反应,临床效果良好,且无移植物相关并发症发生。陈家祺等[45]利用异体脱细胞基质材料对10例眼睑缺损患者进行眼睑原位重建,平均随访8个月显示,脱细胞真皮植入眼睑后炎性反应轻微,未见有植入物脱落和感染现象,受体结膜可在脱细胞真皮表面爬行生长。组织学检查发现术后半年脱细胞真皮植片内有新生毛细血管和纤维母细胞存在。 隆唇:Castor等[46]应用脱细胞基质材料联合自体脂肪行隆唇与单纯应用自体脂肪注射行隆唇对比,结果显示,脱细胞基质材料联合自体脂肪组红唇外露平均增加约61%,而单纯应用自体脂肪组平均增加约13%;随访3个月,脱细胞基质组唇部外翘增加1 mm且无明显吸收,而单纯脂肪注射组有约9%的吸收。Sclafani等[47]用微粉化的脱细胞基质材料注射治疗老年性唇萎缩,发现术后美学效果和长期效果均优于使用胶原蛋白患者。 2.4.6 其他 Witt等[48]将脱细胞基质材料用于治疗大疱性表皮松解症的假性并指,组织学研究表明脱细胞基质材料保留了正常皮肤结构的部分特点,但远期效果仍需进一步随访。杨勇等[49]采用同种异体脱细胞真皮基质作为组织替代物,对8例复杂性膀胱阴道瘘患者进行手术治疗,效果确切,避免了以往获取自体组织所带来的创伤。Zhu等[50]将脱细胞整皮基质作为组织工程生物材料,用于53例Mayer-Rokitansky-Kaster- Hauser综合征患者阴道整形术中,取得了满意效果。 2.5 细胞外基质源脱细胞基质材料在整形外科的应用优势 细胞外基质源材料相对于惰性组织源材料具有更多优势,如免疫原性低,生物相容性好,完全可降解吸收,可与宿区有效整合,主动吸引自体干细胞迁入损伤处并促进增殖和分化而实现部分程度的特异性、功能性修复。其中小肠黏膜下层是一种商业化的细胞外基质源脱细胞基质材料,在普外科、神经外科、胸外科已被广泛应用,并逐渐应用于整形外科中[51]。Macleod等[52]报道称猪真皮来源的脱细胞基质材料在皮下植入20周后,引起一定程度的急性、慢性炎症反应,并形成纤维化包裹,造成降解过程与组织血管化受限,而同组的猪小肠黏膜下层来源的脱细胞基质材料则未发现明显的慢性炎症,组织重建效果良好。美国COOK公司开发的小肠黏膜下层来源脱细胞基质材料用于隆唇整形前瞻性临床试验,100%患者对整形效果表示满意,并有50%患者要求进一步增加填充小肠黏膜下层的用量,6个月临床随访未发现不良反应,结果表明小肠黏膜下层可以为隆唇后的肌肉生长提供三维空间支架结构,将成为一种潜在的高活性整形外科长期填充材料[53]。 "
| [1] Dong J,Gantz M,Goldenberg G.Efficacy and safety of new dermal fillers.Cutis.2016;98(5):309-313. [2] Kim JJ,Evans GR.Applications of biomaterials in plastic surgery.Clin Plast Surg.2012;39(4): 359-376.[3] Lin YQ,Wang LR,Wang JT,et al.New advances in liver decellularization and recellularization: innovative and critical technologies.Expert Rev Gastroenterol Hepatol. 2015;9(9):1183-1191.[4] Gilpin A,Yang Y.Decellularization Strategies for Regenerative Medicine: From Processing Techniques to Applications. Biomed Res Int. 2017; 2017:9831534. [5] 刘文博,高茗.可重塑生物补片在疝及腹壁外科的应用和展望[J].海军医学杂志,2016,37(4):378-381.[6] Deprest J,Klosterhalfen B,Schreurs A,et al.Clinicopathological study of patients requiring reintervention after sacrocolpopexy with xenogenic acellular collagen grafts.J Urol. 2010;183(6):2249-2255.[7] Gaertner WB,Bonsack ME,Delaney JP.Experimental evaluation of four biologic prostheses for ventral hernia repair. J Gastrointest Surg. 2007; 11(10):1275-1285.[8] Chen Y,Chen J,Zhang Z,et al.Current advances in the development of natural meniscus scaffolds: innovative approaches to decellularization and recellularization.Cell Tissue Res.2017;370(1):41-52. [9] Zhang J,Wang GY,Xiao YP,et al.The biomechanical behavior and host response to porcine-derived small intestine submucosa,pericardium and dermal matrix acellular grafts in a rat abdominal defect model. Biomaterials. 2011;32:7086-7095.[10] Harrell AG,Novitsky YW,Kercher KW,et al.In vitro infectability of prosthetic mesh by methiciliin-resistant staphylococcus aureus.Hernia. 2006;10(2):120-124. [11] Srivastva A,DeSagun EZ,Jennings LJ,et al.Use of porcine aeellular dermal matrix as a dermal substitute in rats.Ann Surg. 2001;233(3):400-408.[12] 姜笃银,钱春华,周兵,等.不同脱细胞方法对无细胞真皮基质抗原成分的影响[J].中国临床康复,2005,9(6):35-37.[13] Huai G,Qi P,Yang H,et al.Characteristics of alpha-Gal epitope, anti-Gal antibody, alpha1,3 galactosyltransferase and its clinical exploitation (Review).Int J Mol Med.2016;37(1):11-20.[14] Wu LC,Kuo YJ,Sun FW,et al.Optimized decellularization protocol including alpha-Gal epitope reduction for fabrication of an acellular porcine annulus fibrosus scaffold.Cell Tissue Bank. 2017;18(3):383-396.[15] Wong ML,Wong JL,Vapniarsky N,et al.In vivo xenogeneic scaffold fate is determined by residual antigenicity and extracellular matrix preservation.Biomaterials.2016;92:1-12.[16] Takeo M,Lee W,Ito M.Wound healing and skin regeneration. Cold Spring Harb Perspect Med. 2015;5(1):a23267.[17] Eming SA,Martin P,Tomic-Canic M.Wound repair and regeneration: mechanisms, signaling, and translation.Sci Transl Med. 2014;6(265): 265s-266s.[18] Wainwright D,Madden M,Luterman A,et al.Clinical evaluation of an acellular allograft dermal matrix in fullthickness burns.J Burn Care Rehabil.1996;17(2):124-136.[19] 潘云川,徐家钦,陈彦,等.烧伤早期切痂异体真皮基质与自体皮浆复合移植的临床应用[J].临床运用中华外科杂志, 2004,42(7):410-412.[20] 孙永华,李迟,王春元,等.脱细胞异体真皮与自体薄皮片移植的研究与应用[J].中华整形烧伤外科杂志,1998,14(5):370-373,402.[21] 宁勇,刘明锁,刘文文,等.异种脱细胞真皮基质覆盖自体微粒皮治疗大面积深度烧伤疗效观察[J].山东医药,2014,54(44):91-92.[22] 黄智勇,陈大夫,王晓,等.异体脱细胞真皮基质在烧伤后遗畸形中的应用[J].中国美容医学,2006,15(7):772-774.[23] 霍然,付洪滨,吕仁荣,等.脱细胞真皮基质在胸部瘢痕疙瘩治疗中的应用[J].中国临床康复,2004,18(4):474.[24] Gibbs S,van den Hoogenband HM,Kirtschig G,et al.Autologous fullthickness skin substitute for healing chronic wounds. Br J Dermatol. 2006;155(2):267-274.[25] Godwin J,Kuraitis D,Rosenthal N.Extracellular matrix considerations for scar-free repair and regeneration: insights from regenerative diversity among vertebrates.Int J Biochem Cell Biol.2014;56:47-55.[26] 陈颖,陈嘉健,陈嘉莹,等.中国乳腺癌术后乳房重建现况调查报告[J].中华肿瘤杂志,2014,36(11):851-857.[27] Dong JY,Yan Y,Liu MF,et al.Use of Acellular Dermal Matrices in One-stage Implant-based Breast Reconstruction.Zhongguo Yi Xue Ke Xue Yuan Xue Bao.2016;38(5):607-610.[28] Jin US,Hong KY,Hwang YI.Effect of adipose-derived stem cells on acellular dermal matrix engraftment in a rabbit model of breast reconstruction.J Plast Reconstr Aesthet Surg. 2017;70(6):806-813.[29] Nafisi N,Akbari ME,Mahjoub F,et al.Application of Human Acellular Breast Dermal Matrix (ABDM) in Implant-Based Breast Reconstruction: An Experimental Study.Aesthetic Plast Surg. 2017;41(6):1435-1444. [30] Spear SL,Sher SR,Al-Attar A,et al.Applications of acellular dermal matrix in revision breast reconstruction surgery.Plast Reconstr Surg. 2014;133(1):1-10.[31] Long X,Bai M,Zeng A,et al.Application of acellular allograft dermal matrix in breast implants for secondary breast deformity post polyacrylamide hydrogel removal.Zhongguo Yi Xue Ke Xue Yuan Xue Bao.2014;36(5):530-533.[32] Paprottka FJ,Krezdorn N,Sorg H,et al.Evaluation of Complication Rates after Breast Surgery Using Acellular Dermal Matrix: Median Follow-Up of Three Years.Plast Surg Int.2017;2017:1283735.[33] Zenn M,Venturi M,Pittman T,et al.Optimizing Outcomes of Postmastectomy Breast Reconstruction With Acellular Dermal Matrix: A Review of Recent Clinical Data. Eplasty. 2017;17:e18.[34] Krishnan NM,Chatterjee A,Rosenkranz KM,et al.The cost effectiveness of acellular dermal matrix in expander-implant immediate breast reconstruction.J Plast Reconstr Aesthet Surg. 2014;67(4):468-476.[35] Utomo L,Pleumeekers MM,Nimeskern L,et al.Preparation and characterization of a decellularized cartilage scaffold for ear cartilage reconstruction.Biomed Mater.2015;10(1):15010.[36] Luan J,Cai Z,Yang P.Culture of chondrocytes using allogenous acellular cartilaginous matrix. Zhonghua Zheng Xing Shao Shang Wai Ke Za Zhi.1999;15(3):178-179.[37] Zhang C,Jing S,Yang K,et al.Cartilage tissue engineering with acellular cartilage matrix as scaffold in rabbit model. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2008;22(7):846-850.[38] Clark JM,Saffold SH,Israel JM.Decellularized dermal grafting in cleft palate repair. Arch Facial Plast Surg.2003;5(1):40-44.[39] Cole P,Horn TW,Thaller S.The use of decellularized dermal grafting(AlloDerm) in persistent oro-nasal fistulas after tertiary cleft palate repair.J Craniofac Surg.2006;17(4):636-641.[40] 李光强,蒲兴旺,邵文辉.脱细胞异体真皮基质医用组织补片在隆鼻术中的应用体会[J].中国美容医学,2007,16(12):1661-1662.[41] Suh MK,Lee KH,Harijan A,et al.Augmentation Rhinoplasty With Silicone Implant Covered With Acellular Dermal Matrix.J Craniofac Surg.2017;28(2):445-448.[42] Jackson IT,Yavuzer R.AlloDerm for dorsal nasal irregularities.Plast Reconstr Surg.2001;107(2):553-558. [43] Gryskiewicz JM,Rohrich RJ,Reagan BJ.The use of alloderm for the correction of nasal contour deformities.Plast Reconstr Surg. 2001; 107(2):561-570.[44] Shorr N,Perry JD,Goldberg RA,et al.The safety and applications of acellular human dermal allograft in ophthalmic plastic and reconstructive surgery:a preliminary report.Ophthal Plast Reconstr Surg.2000;16(3):223-230.[45] 陈家祺,顾建军,彭鸿钧,等.应用同种异体脱细胞真皮的眼睑原位重建术[J].中华眼科杂志,2005,5(3):56-57.[46] Castor SA,To WC,Papay FA.Lip augmentation with alloderm acellular allogenic dermal graft and fat autograft:A comparison with autologous fat injection alone.Aesthetic Plast Surg. 1999;23(3):218-223.[47] Sclafani AP,Romo T 3rd,Jacono AA.Rejuvenation of the aging lip with an injectable acellular dermal graft(Cymetra).Arch Facial Plast Surg. 2002;4(4):252-257.[48] Witt PD,Cheng CJ,Mallory SB,et al.Surgical treatment of pseudosyndactyly of the hand in epidermolysis bullosa: histological analysis of an acellular allograft dermal matrix.Ann Plast Surg. 1999; 43(4):379-385.[49] 杨勇,许勇,徐峰,等.同种异体脱细胞真皮基质在膀胱阴道瘘修补术中的应用[J].中国临床保健杂志,2007,10(2):135-136.[50] Zhu L,Zhou H,Sun Z,et al.Anatomic and sexual outcomes after vaginoplasty using tissue-engineered biomaterial graft in patients with Mayer-Rokitansky-Kuster-Hauser syndrome: a new minimally invasive and effective surgery.J Sex Med. 2013;10(6):1652-1658.[51] Zhang L,Du A,Li J,et al.Development of a cell-seeded modified small intestinal submucosa for urethroplasty.Heliyon. 2016;2(3):e00087. [52] Macleod TM,Williams G,Sanders R,et al.Histological evaluation of Permacol as a subcutaneous implant over a 20-week period in the rat model.Br J Plast Surg. 2005;58(4):518-32.[53] Seymour PE,Leventhal DD,Pribitkin EA.Lip agmentation with porcine small intestinal submucosa. Arch Facial Plast Surg.2008;10(1):30-33. |
| [1] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [2] | Liu Zhigang, Guo Qinggong, Chen Jingtao. Effect of Capparis spinosa total alkaloid on proliferation and apoptosis of nucleus pulposus cells in an intervertebral disc degeneration rat model [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1699-1704. |
| [3] | Luo Yaxin, Bi Haoran, Chen Xiaoxu, Yang Kun. Extracellular matrix and tissue engineering regeneration and repair [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1785-1790. |
| [4] | Li Junqi, Tian Guangzhao, Chen Mingxue, Wang Hao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Li Ming, Guo Quanyi. Regulatory effect of acellular cartilage extracellular matrix on phenotype of mouse macrophage line [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(10): 1512-1516. |
| [5] | Guo Haoyu, Li Weiquan, Liu Kaiyuan, Xiao Ruifen, Sun Denglong, Xi Jiaoya. Recent research progress in construction of biomimetic engineered cardiac tissue based on extracellular matrix [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(10): 1577-1584. |
| [6] | Fan Xuemin, Fang Shanbao, Chen Zhixing, Mo Shuixue. Status and application prospects of nano-clay Laponite [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(10): 1622-1627. |
| [7] | Wu Ming, Zhang Yan. Related factors regulating osteogenic differentiation of bone marrow mesenchymal stem cells through Wnt/β-catenin signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(1): 116-122. |
| [8] | Ren Chunmei, Liu Yufang, Xu Nuo, Shao Miaomiao, He Jianya, Li Xiaojie. Non-coding RNAs in human dental pulp stem cells: regulations and mechanisms [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(7): 1130-1137. |
| [9] | Liu Chunyu, Han Xiaoyan, Wang Lin. Basic science related to tendinopathy: microbiomechanics and stress shielding [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 766-772. |
| [10] | Wang Zhihao, Wu Cong, Wu Sihua, Shi Hongcan. Application and characteristics of decellularization technology in tissue engineered trachea [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(35): 5695-5700. |
| [11] | Yang Wenxiao, Yang Ning, Liu Yao. Immunomodulation of extracellular matrix and its role in tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(35): 5701-5707. |
| [12] | He Jing, Ao Qiang. Research hotspots in tissue decellularization method for manufacturing extracellular matrices [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5413-5420. |
| [13] | Zhou Pengfei, Lin Jing, Chen Yuying, Lin Minkui. Canine dental pulp stem cells-polyglycolic acid scaffold complex for canine periodontal tissue defect [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5526-5531. |
| [14] | Cheng Xue, Fang Hong, Zhang Yunke, Wu Yingen. Interventional mechanism of Feibi prescription on extracellular matrix transformation in a mouse model of pulmonary fibrosis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 5038-5043. |
| [15] | Liu Guoming, Wang Qinfen, Lin Kefeng, Zhou Shiguo, Chen Zuxing, Lin Shishui. Whole body application of nerve growth factor promotes early healing of tibial shaft fracture and improves expression of bone morphogenetic protein-2 and vascular endothelial growth factor in rats [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(29): 4680-4685. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||